חוקרים מהמרכז הרפואי שיבא תל השומר ומאוניברסיטת תל אביב גידלו לראשונה בעולם מרכיבי כליה עוברית אנושית מתאי גזע רקמתיים. הכליה גדלה והתפתחה במקביל למתרחש ברחם הן מבחינת משך הזמן והן מבחינת התהליכים ובכך אפשרה לחוקרים לראות בזמן אמת את התפתחות האיבר, לבודד גנים שמובילים למומים מולדים, לפתח טיפולים חדשניים בתחום הרפואה הרגרנטיבית ולבדוק רעילות של תרופות בהיריון על כליות עוברים.
המחקר פורץ הדרך נערך בהובלת פרופ' בנימין דקל, נפרולוג וחוקר בעל שם עולמי, מנהל היחידה לנפרולוגיה ילדים והמכון לחקר תאי אב בבית החולים לילדים ע"ש ספרא במרכז הרפואי שיבא ומנהל מרכז סגול לרפואה רגנרטיבית באוניברסיטת תל אביב. במחקר השתתפו גם הדוקטורנט ד"ר מיכאל נמסטניקוב, בוגר מסלול רופא-חוקר בפקולטה לרפואה באוניברסיטת תל אביב, וד"ר אוסנת כהן-זונטג, עמיתת מחקר במרכז הרפואי שיבא, כחלק מקבוצת המחקר של פרופ' דקל.
תוצאות המחקר התפרסמו בכתב העת היוקרתי The EMBO Journal.
"החיים מתחילים עם תאי גזע פלוריפוטנטיים, שיכולים להתמיין לכל תא בגוף", מסביר פרופ' דקל. "בעבר הצליחו לגדל אורגנואידים – תרביות תלת-ממדיות דמויות-איברים – על ידי הפקת תאי גזע כלליים כאלה ומיונם לכליות, אבל אחרי חודש לערך הכליה בתרבית מתה, והיה צריך להתחיל בתהליך שוב. לפני כעשור קבוצת המחקר שלי הצליחה לבודד לראשונה את תאי הגזע הרקמתיים של הכליה האנושית שאחראים לגדילת האיבר. הבנו שעל מנת לגדל את האורגנואיד הכלייתי בתלת-ממד יש לשמור על קיומם של תאי הגזע הרקמתיים בתרבית, כך פעלנו וכעת הצלחנו לראשונה לגדל כליה אנושית בצורת אורגנואיד מתאי הגזע הספציפיים של הכליה וזאת במקביל לתהליך ההבשלה ברחם הקורה עד שבוע 34 של הריון. זה הישג שבין היתר מראה שהתאים שבודדנו אכן היו תאי הגזע הרקמתיים של הכליה, שכן הם התמיינו, התארגנו לרקמה ובנו את הכליה בהצלחה במעבדה".
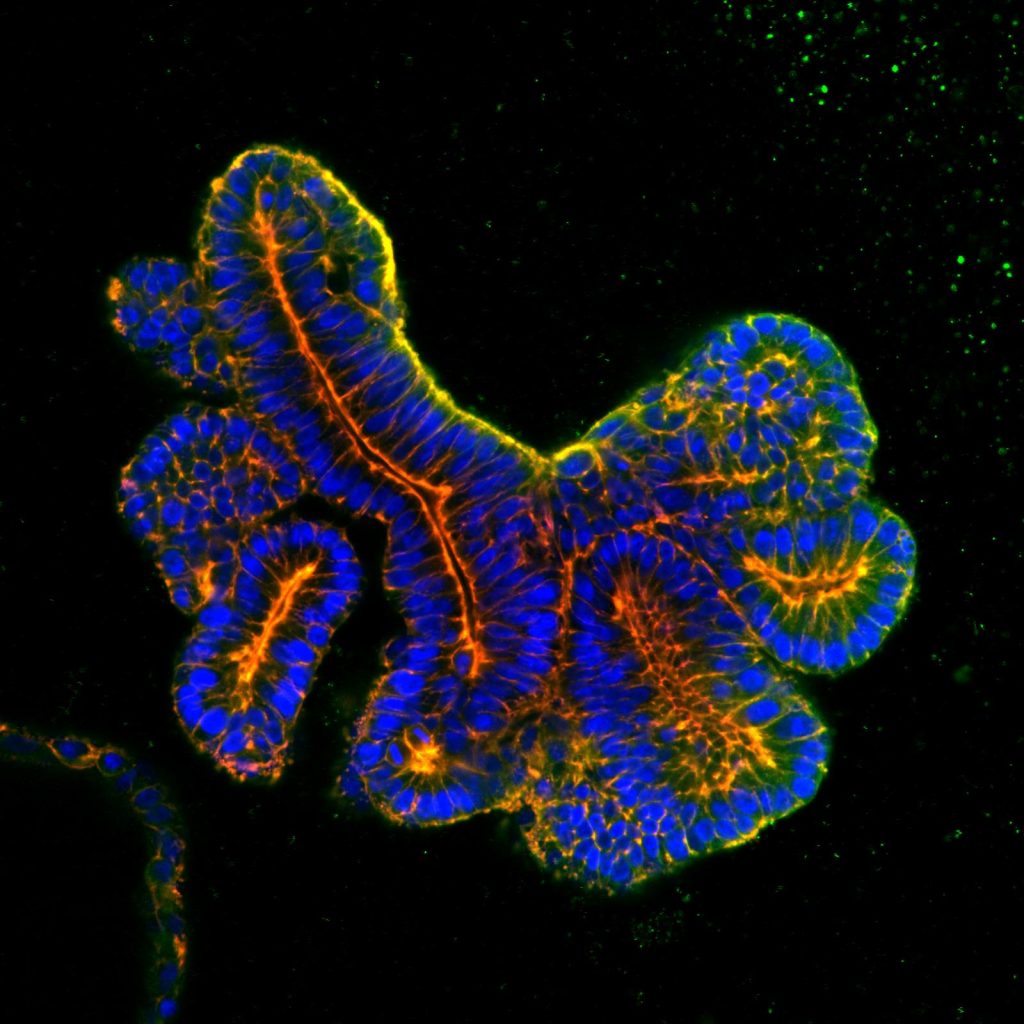
צוות המחקר מסביר כי חוקרים מגדלים אורגנואידים בתנאי מעבדה כדי לחקור איברים באופנים שאינם מתאפשרים בבני אדם, אלא שאורגנואידים שמקורם מתאי גזע פלוריפוטנטיים עלולים עקב תהליך התמיינות לא שלם להכיל תאים לא רצויים שאינם קשורים לאיבר הנלמד ועלולים להתרחק מהמקור. לעומת זאת, אורגנואיד הכליה שצמח מתאי גזע רקמתיים של כליה עשה זאת באופן "נקי", שכן תאי גזע אילו מתוכנתים בטבע להתמיין אך ורק לרקמת כליה. תאים אלה התמיינו לסוגים שונים של תאי כליה, ויצרו לאורך 34 שבועות רקמות שונות של הכליה, כמו מסנני דם וצינורות שתן.
"האפשרות לגדל כליה עוברית למשך זמן השווה לזמן שבו הכליה צומחת בהיריון יכולה לשפוך אור חדש על תהליכים ביולוגיים בכלל, ובפרט על תהליכים שמובילים למחלות כליה", אומר פרופ' דקל. "כיום כדי ללמוד על מום מולד זה או אחר, משתמשים בעכברים: משנים להם גן זה או אחר, ועוקבים אחר ההתפתחות. אבל בסופו של דבר מדובר בעכבר, לא באדם. מן הסתם איננו יכולים לשחק עם גנים של עוברים בהיריון. לעומת זאת, אורגנואיד כליה במעבדה אין בעיה לחקור, במיוחד אם מסלולי האותות של ההתפתחות זהים למקור כפי שנמצא בטכנולוגיה שפיתחנו. ובאמת כשחסמנו בצורה נקודתית מסלול אותות מסוים, ראינו איך בצד השני הוא מוביל למום מולד. אנחנו ממש רואים בלייב איך בעיה בהתפתחות מובילה למחלת כליות שרואים בקליניקה מה שיאפשר פיתוח טיפולים חדשניים".
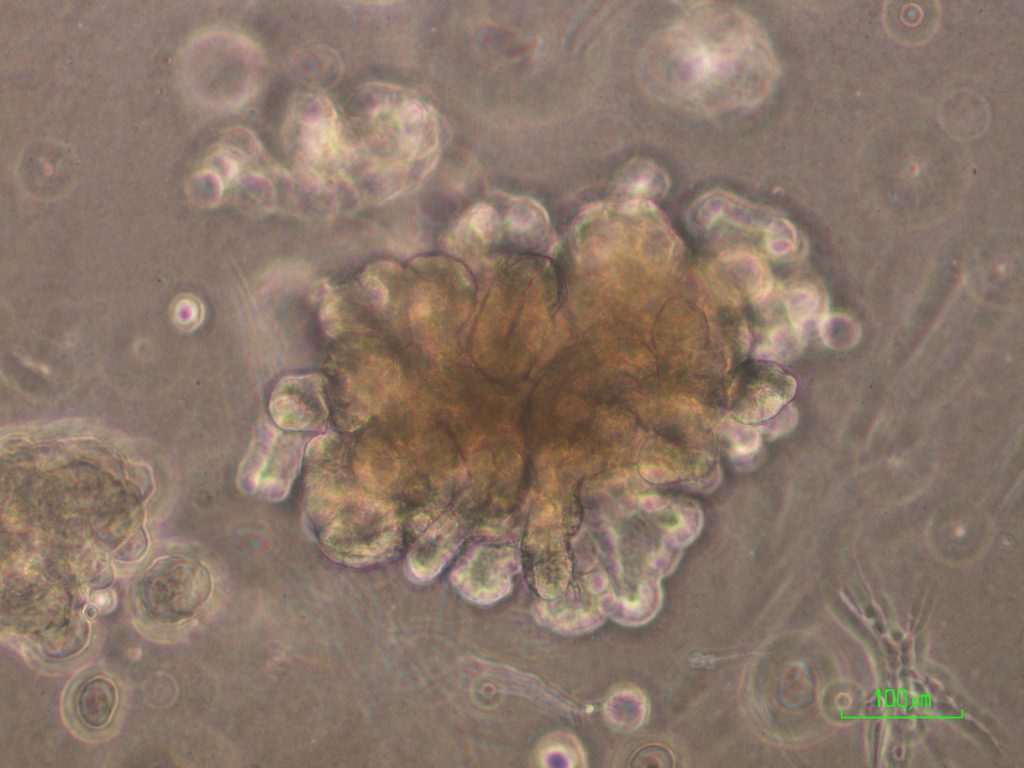
פרופ' דקל מדגיש כי לפריצת הדרך השלכות החורגות בהרבה ממדע בסיסי, כלומר מההבנה הביולוגית של התפתחות הכליה. "העובדה שאנחנו יכולים לגדל לאורך זמן תאי גזע רקמתיים של כליה מחוץ לגוף פותחת פתח לרפואה רגנרטיבית, כלומר להשתלת רקמות כליה שגודלו במעבדה – בתוך הגוף. כעת יש לנו למעשה מקור בלתי נדלה של תאים כלייתיים שונים, והבנה טובה יותר של תפקידיהם השונים בהתפתחות ובתפקוד הכליה.
פרט לכך אנחנו יכולים להשתמש באורגנואיד שלנו כדי לבדוק רעילות של תרופות. נשים בהיריון נוטלות תרופות, כמו למשל סוגים שונים של אנטיביוטיקה למרות שלא תמיד אנו יודעים בוודאות מה הן עושות לעוברים אנושיים. כמובן שבודקים תרופות על בעלי חיים – אבל זה לא עונה על השאלה. האורגנואיד שלנו מאפשר לבדוק את התרופות על כליה שמדמה בצורה אמינה כליה של עובר אנושי, ובנקודות זמן שונות לאורך ציר התפתחותו. בעתיד הקרוב אנחנו רוצים לשכלל את האורגנואיד שלנו, ולהוסיף לו רשת כלי דם, שתוסיף ממד נוסף של מורכבות – ותתקרב עוד יותר לדבר עצמו. לשם כך גייסנו חוקר נוסף המתמחה ביצירת רשתות כלי דם למרכז סגול לרפואה רגנרטיבית אשר משתלב במטרות המרכז של הצמחת, שיקום והצערת איברים".
פרופ' דרור חרץ, יו"ר רשות המחקר בשיבא: "חשיבותו של המחקר איננה רק בהישג המדעי יוצא הדופן, אלא גם בחיזוק מעמדה של ישראל בחזית המדע העולמית. בשנים האחרונות אנו עדים לניסיונות להרחיק את ישראל ממוקדי ההשפעה הבינלאומיים, והצלחות מדעיות מהסוג הזה הן תזכורת לכך שתרומתנו למחקר הרפואי והמדעי היא משמעותית ובלתי ניתנת לערעור".
אנו מכבדים זכויות יוצרים ועושים מאמץ לאתר את בעלי הזכויות בצילומים המגיעים לידינו .אם זיהיתם בפרסומנו צילום אשר יש לכם זכויות בו , אתם רשאים לפנות אלינו ולבקש לחדול מהשימוש באמצעות המייל info@rgg-news.co.il






